1. 「好中球数減少」は自然免疫における重要なバリア
化学療法中の経過において、好中球数減少(neutropenia)は感染症発症における重要なリスク因子の一つです。
歴史的にも、好中球数減少の程度と感染リスクの相関は古くから指摘されており、好中球数減少は自然免疫における生体防御の破綻を示す数的指標として扱われてきました。
固形臓器悪性腫瘍患者に使用される抗がん化学療法レジメンでの好中球減少の程度はそれほど強くありませんが、血液悪性腫瘍患者、特に造血幹細胞移植や急性骨髄性白血病における前処置および寛解導入/地固め化学療法では状況が異なります。
これらは好中球減少の程度が強く、さらにその期間も長いことが特徴です。
また、これらの強力な抗がん化学療法レジメンは口腔内や消化管粘膜の破綻も来たすため、自然免疫である「バリア」と「好中球」は合わせて障害されることが多いです。
特に、重度の好中球数減少下で発症する発熱性好中球減少症(FN: febrile neutropenia)は、迅速な治療介入を要する内科的エマージェンシーとして確立された臨床概念です。
一方、感染症リスクを規定する要因は好中球の「数」だけで説明できないことも明らかになっています。
実際には、好中球の機能の低下や、粘膜バリアをはじめとする他の防御機構の破綻が複雑に関与しています。
本稿では、好中球数減少を総合的に評価するための視点について解説します。
2. 好中球の役割:自然免疫における中心的細胞
好中球は、生体内に侵入した病原体を即座に排除する自然免疫の中心的な役割を持つ細胞です。
その基本機能は、走化(chemotaxis)、貪食(phagocytosis)、そして殺微生物活性(microbicidal activity)の三段階に分かれます。
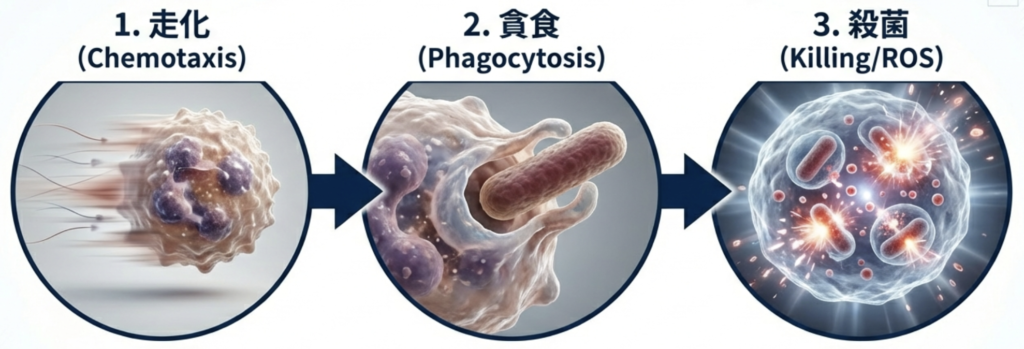
まず、細菌や真菌が侵入すると、補体成分C5aやインターロイキン-8(IL-8)などの化学走化因子に誘導され、好中球は炎症部位へと迅速に動員されます。
現場に到達した好中球は、補体や抗体でオプソニン化された病原体を認識し、細胞内へ取り込みます。
その後、活性酸素種(ROS: reactive oxygen species)を産生する呼吸バーストや、顆粒内に含まれる強力な殺菌タンパク質を放出することで、病原体を破壊します。
好中球が欠損、あるいは機能不全に陥ると、侵入した病原体は局所での制御を免れ、容易に増殖を開始します。
その結果、組織侵入から血行性播種、さらには致命的な敗血症へと急速に進展する危険性が高まります。
このため、細菌や真菌に対する初期防御において、好中球は重要な役割を果たしているのです。
3. 好中球減少の定義と臨床的重症度
固形臓器悪性腫瘍患者の抗がん化学療法による好中球減少期間は一般的に7日以内であるのに対して、血液悪性腫瘍患者への化学療法の場合は14日以上持続することもあります。
日本臨床腫瘍学会によると、FNは「腋下温37.5度以上の発熱があり、好中球数<500/μLまたは<1000/μLで48時間以内に<500μLになることが予測される」という条件を満たし、主に化学療法による骨髄抑制の結果としての好中球減少期の発熱と定義されています。
米感染症学会、欧州臨床腫瘍学会、日本臨床腫瘍学会によって若干定義が異なりますが、概ね同様の概念です。
固形臓器悪性腫瘍患者では5-30%、血液悪性腫瘍患者では80%以上でFNに至ると言われています。
FNは悪性腫瘍患者における内科的緊急症であり、診断後は迅速な抗菌薬の開始が求められます。
診断後1時間以内、特に30分以内の治療開始が推奨されており、その後1時間遅れるごとに28日死亡率が18%上昇するという報告もあります。

FNの定義とは別に、Common Terminology Criteria for Adverse Events (CTCAE) version 5.0という抗がん剤関連合併症のグレーディングに使われるツールでは好中球数絶対数(ANC)が1500-500/mm³をgrade1-3の好中球数減少、500/mm³未満をgrade4の好中球数減少としています。
更に血液悪性腫瘍で用いられる強力な化学療法では100/mm³未満に至ることも多々あり、米国感染症学会の定義ではこれを高度好中球数減少(profound neutropenia)と定義します。
これを反映して、CTCAE version 6.0の好中球数減少の項目ではgrade3が500-100/mm³、grade4が100/mm³未満のカテゴリーとなりました。
感染発症リスクは、好中球数減少の**「深さ」と「持続期間」**により定量化されます。
特に、ANCが100/mm³未満の状態が7〜10日間以上持続する場合、発熱の頻度はほぼ100%に達し、感染関連死亡リスクも期間に比例して上昇します。
この状態を高度・長期好中球数減少と呼び、CTCAE version 5.0で規定されるgrade4好中球数減少の中でも、特に重篤な状態を指し、一般最近感染症だけでなく侵襲性真菌感染症も考慮しなければならない患者背景です。
好中球による微生物監視機構が失われることで、通常は無害な常在菌でさえ容易に血流へ侵入し、好中球数減少が長期間持続するほど、宿主は極めて脆弱な状態に置かれます。
4. なぜ好中球減少では感染が顕在化しなくなるのか
好中球減少患者の診療における最大の問題は、感染症の兆候が「顕在化しにくい」点にあります。
通常、感染部位では好中球の集積によって発赤、腫脹、膿形成といった典型的な炎症反応が生じますが、好中球が欠乏している状況ではこれらの反応が十分に成立しません。
例えば、肺炎であっても初期には画像上の浸潤影が不明瞭であったり、尿路感染症であっても尿中に膿尿が認められなかったりすることがあります。
また、炎症反応の欠如により局所症状が非特異的となり、発熱のみが唯一かつ最重要の手がかりとなる場合も少なくありません。
さらに、検体中の白血球数が少ないことで、培養や鏡検の感度が低下し、診断の遅れを招く背景もあります。
このように、通常の診断プロセスが通用しにくいことが、好中球減少患者が発熱した場合に迅速な経験的治療が求められる理由となっています。
5. 好中球数だけでは不十分:好中球「機能低下」という視点
好中球の「数」が保たれていても、その「機能」が低下していれば、感染症リスクは明らかに上昇します。
2010年版の米国感染症学会(IDSA)ガイドラインでは、この状態を 機能的好中球数減少(functional neutropenia) と呼び、骨髄異形成症候群(MDS)や急性骨髄性白血病(AML)など、疾患そのものによって循環血中好中球に質的欠陥(貪食能や殺菌能の障害)が生じている状態と定義しています。
実臨床においても、こうした患者は好中球数が正常範囲にあっても感染症に対して極めて脆弱であり、好中球減少患者と同様にハイリスク群として管理する必要があります。
抗がん剤や放射線治療は、骨髄抑制を介して好中球数を減少させるだけでなく、生存している成熟好中球に対しても、遊走能・貪食能・殺微生物活性といった機能を直接的に低下させることが知られています。
また、副腎皮質ステロイドの使用は末梢血中の好中球数を増加させますが、これは血管壁への接着能を抑制し、マージナリングプールから循環血中へ動員しているに過ぎません。実際には、炎症部位への集積、貪食、細胞内殺菌といった機能は抑制されており、見かけ上の好中球数増加とは裏腹に、生体防御能は著しく低下しています。
近年では、特定の分子標的薬もこの「質的な好中球機能不全」に関与することが明らかになっています。
例えば、B細胞受容体シグナル伝達阻害薬であるイブルチニブ(ibrutinib)は、当初の想定を超えて単球や好中球におけるBTK経路も阻害し、侵襲性アスペルギルス症をはじめとする日和見感染症のリスクを高めることが臨床的に報告されています。
さらに、低栄養や微量元素(鉄など)の異常も、好中球の殺菌プロセスに不可欠な活性酸素産生を阻害し、宿主を重層的な感染リスクにさらす要因となります。
このように、疾患背景や治療介入によって「数はあっても機能しない好中球」という状況が生じ得るため、単なる好中球数の評価にとどまらず、患者が受けている治療内容や宿主因子を踏まえた質的な評価が不可欠です。
しかし現時点では、好中球機能を臨床的に定量評価する標準的手法や、発熱性好中球減少症(FN)のように確立された治療戦略は存在せず、臨床判断は依然として経験的要素に依存しているのが現状です。
6. 好中球減少と関連する病原微生物
好中球減少下では、特定の防御機構が失われることで、問題となる病原体のスペクトラムが拡大・変化します。
好中球は微生物の種類を選ばずに作用する非特異的な自然免疫の主力因子であるため、その欠損は、通常は病原性が低いとされる環境微生物や常在菌に対しても生体への「侵入門戸を開く」ことになります。
主に以下の病原体が重要です。
グラム陽性球菌:
現在の臨床現場で最も頻繁に血液から分離されるのは、コアグラーゼ陰性ブドウ球菌(CoNS)です。
これらは皮膚常在菌ですが、血管カテーテルなどのデバイス挿入によって物理的バリアが突破されることで血流へ侵入し、カテーテル関連血流感染症(CLABSI)の主要な原因となります。
一方、黄色ブドウ球菌(Staphylococcus aureus)は、CoNSに比べて病原性が高く、重症感染症を引き起こすリスクがあるため、迅速な対応が求められます。
さらに、口腔内常在菌であるViridans群連鎖球菌(VGS)はFNにおいて非常に重要な微生物です。この微生物群は抗がん剤による粘膜バリア障害(MBI)を契機に血流へ侵入し、敗血症性ショックや急性呼吸窮迫症候群(ARDS)といった致死的な合併症を引き起こすことがあります。
この重篤な病態は黄色ブドウ球菌によるtoxic shock syndromeに類似した『toxic shock–like syndrome』と呼ばれ、好中球減少を伴う菌血症患者の最大25%に認められることがあります。
また、がん患者で検出されるVGSはペニシリンに耐性率が高く、更にフルオロキノロンへの感受性も低下しています。
そのため、重度の粘膜障害がある患者でショックやARDSの兆候が見られる場合には、初期の経験的治療にバンコマイシンを早期に組み込むことが、予後の改善において極めて重要です。
グラム陰性桿菌:
大腸菌(E. coli)、肺炎桿菌(K. pneumoniae)、および緑膿菌(P. aeruginosa)が代表的であり、これらは主に宿主の消化管内に定着しています。
化学療法による粘膜バリア障害(MBI)が生じると、これらの菌が血流内へ侵入する「トランスロケーション」が起こり、感染が成立します。
好中球減少患者におけるグラム陽性球菌による菌血症の死亡率が5%であるのに対し、グラム陰性桿菌では18%に達しており、極めて予後不良です。
なかでも緑膿菌は、初期対応において最も警戒すべき標的です。
歴史的に、好中球減少症における初期経験的治療の推奨薬剤は、「緑膿菌感染に伴う極めて高い死亡率」48時間(2日)以上遅れることは、30日死亡率の増加と有意に関連していることが実証されています。
好中球という「排除の要」を欠いた宿主において、緑膿菌は組織侵襲から重症感染症へと至るスピードが非常に速いため、起因菌の判明を待つ猶予はありません。
そのため、IDSAガイドラインを含むすべての管理戦略において、緑膿菌を確実にカバーする広域β-ラクタム薬の迅速な投与が、生命予後を改善するための絶対的な標準治療として位置づけられています。
真菌:
カンジダ属は、口腔や消化管粘膜のバリア破綻を契機に血流感染症を引き起こします。
これに対し、アスペルギルス属などの糸状真菌は、環境中の胞子を吸入することで感染が始まりますが、その初期防御には好中球が決定的な役割を果たしています。
そのため、ANC 100/mm³未満の重度な好中球減少が2週間以上持続するようなハイリスク患者では、致死的な侵襲性アスペルギルス症のリスクが著しく高まります。
近年は、フルオロキノロン系抗菌薬による予防投与の普及などにより、細菌の耐性パターンが大きく変化しています。
予防投与はグラム陰性桿菌による感染を減少させた一方で、耐性VGSの選択を招く要因ともなっています。
また、MRSA(メチシリン耐性黄色ブドウ球菌)VRE(バンコマイシン耐性腸球菌)、ESBL(基質特異性拡張型β-ラクタマーゼ)産生菌、CRE/CPE(カルバペネム耐性/カルバペネマーゼ産生腸内細菌目細菌)などの多剤耐性菌の増加が、現在の診療における大きな脅威となっています。
7. 好中球減少患者の評価と臨床推論のポイント
好中球減少患者の診療では、まずANCの深さと持続期間を評価し、感染リスクの全体像を把握します。
その上で、その急速な病状悪化を来たす可能性があることから。「発熱 = 感染症の発症」と考え、起因菌が同定される前であっても迅速に広域抗菌薬による経験的治療を開始します。
身体所見や画像診断が重要であることは免疫不全以外の患者と同様非常に重要な情報ですが、その限界を理解し、わずかな症状変化を見逃さない慎重な観察が求められます。
また、粘膜障害の有無や血管カテーテルの存在など、病原体の侵入経路を個別に評価し、想定される病原体を絞り込みます。
最終的には、検出された微生物から逆算して宿主防御機構のどこに欠損があるのかを再評価する、双方向的な臨床推論が重要となります。
8. まとめ
好中球数は、免疫不全患者における感染症診療の最も基本的かつ重要な評価基準です。
一方で、”好中球数減少+発熱があれば広域抗菌薬を開始する”という一見単純なアプローチであるが故に、好中球減少の本質的な意味を見落としがちになる危険性も孕んでいます。
発熱性好中球減少症(FN)は、あくまで表現型であり、その実を示すものでは決してないことを認識する必要があります。
不慣れな医療従事者向けの啓発としてこの単純なアプローチは有効ではあるものの、その後の継続的なマネジメントを担う血液内科医、感染症科医や集中治療医は、好中球減少の背後にある多層的な免疫障害を理解し、立体的に患者を評価する視点を持つことが求められます。


