1. なぜ「細胞性免疫」として独立的に捉える必要があるのか
自然免疫(バリアや好中球)は、侵入した微生物を抗原非特異的に、かつ迅速に排除しようとする生体防御の最前線です。
一方で、主にTリンパ球が担う細胞性免疫は、生体防御全体を制御する「司令塔」としての役割を果たします。
細胞性免疫の最大の特徴は、その抗原特異性と、免疫応答全体をorchestration(統合・調整)する能力にあります。
T細胞は、遺伝子再構成によって多様性を獲得したT細胞受容体(TCR)を用いて特定の抗原を認識します。
そのうえで、抗原特異性を持たないマクロファージや好中球などの自然免疫細胞を動員・活性化し、それらの抗菌活性を状況に応じて高度に制御します。
この防御様式の違いは、感染症の臨床像に直接反映されます。
好中球を含む自然免疫は、侵入した病原体をどれだけ迅速かつ大量に排除できるかという点で機能する防御機構であり、いわば量的防御として捉えることができます。
これが障害されると、病原体の初期排除が不十分となり、局所感染から敗血症へと急速に進展する急性細菌感染や侵襲性真菌症のリスクが前面に出てきます。
これに対して、細胞性免疫は、どの病原体を長期的に制御できるかという点で機能する防御機構であり、質的防御として位置づけることができます。
その機能が低下すると、ウイルス、結核菌、特定の真菌や寄生虫といった細胞内寄生体が制御不能となり、感染症の臨床像は急性期の病態から、「潜伏感染」や「再活性化」を主体とする病態へと質的に変化します。
T細胞は、CD4陽性T細胞が食細胞を活性化して細胞内寄生菌や真菌を制御し、CD8陽性T細胞がウイルス感染細胞を直接殺傷することで、病原体が体内で複製・生存するための環境そのものを断ち切ります。
したがって、細胞性免疫が障害されると、生体は病原体の「封じ込め(disease containment)」に失敗します。
その結果、通常であれば無症候性で経過する、あるいは軽微な症状にとどまる感染症が、重篤化・慢性化・再発を繰り返す臨床像へと変貌します。
2. 細胞性免疫(T細胞)の基本的役割の整理
T細胞は、抗原提示細胞(antigen-presenting cell:APC)によって、主要組織適合遺伝子複合体(MHC)分子を介して提示された抗原を認識することで活性化・分化し、状況に応じたエフェクター機能を発揮します。
この過程を通じて、T細胞は自然免疫細胞と連携しながら、生体防御応答の方向性と強度を制御します。
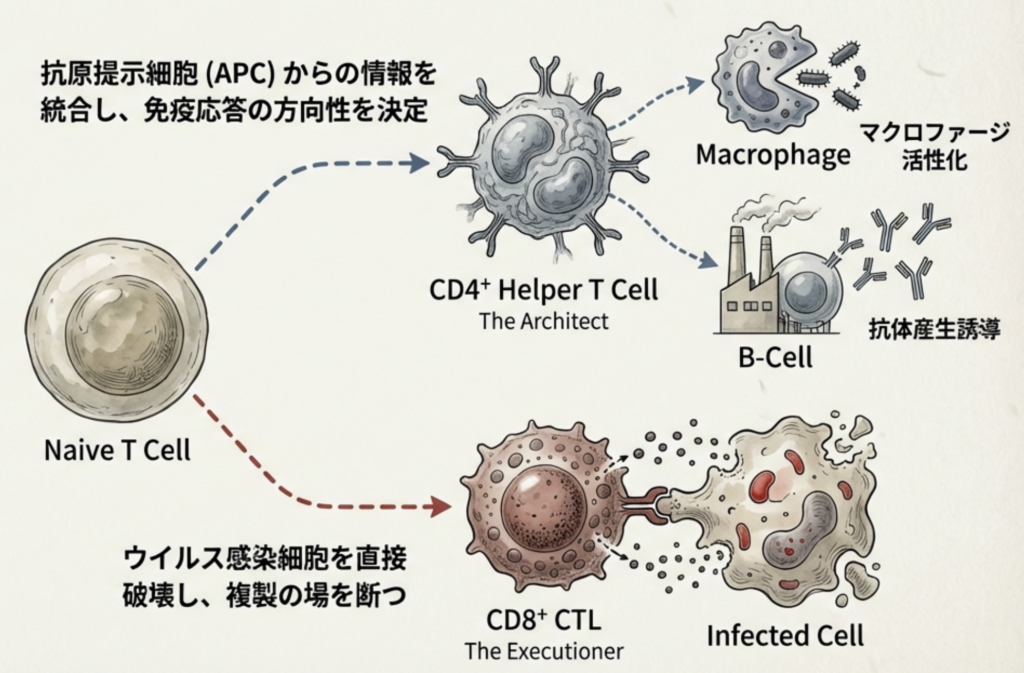
CD4⁺ T細胞(ヘルパーT細胞)
CD4⁺ T細胞は、主に樹状細胞、マクロファージ、B細胞などのAPCが MHC class II 分子を介して提示した抗原を認識することで活性化され、直接微生物を殺傷するのではなく、サイトカインを介して免疫応答全体を調整する役割を担います。
とくに Th1 細胞が産生する IFN-γ は、マクロファージの殺菌能を増強するうえで不可欠であり、結核菌をはじめとする細胞内寄生微生物や一部の真菌に対する防御の中核をなします。
一方、Th2 細胞は、IL-4、IL-5、IL-13 などのサイトカインを介して B 細胞の活性化やクラススイッチを誘導し、抗体産生を促進することで液性免疫を制御します。
このTh2 – B細胞連関は、寄生虫感染に対する防御のみならず、抗体依存性の病原体排除や免疫記憶の形成においても重要な役割を担っています。
B細胞側もAPCとしてT細胞応答を制御する側面も有しているため、共刺激分子(CD80/CD86)を介して CD4⁺ T細胞を活性化・分化へと導き、双方向的に作用します。
さらにTh17 細胞は、粘膜部位において好中球を動員するケモカイン産生を促進し、細胞外細菌や真菌(特にアスペルギルス)に対する局所防御に重要な役割を果たします。
CD8⁺ T細胞(細胞障害性T細胞;CTL)
CD8⁺ T細胞は、ウイルス感染細胞や腫瘍細胞などの多くの有核細胞が有する MHC class I 分子を介して提示する内因性抗原(細胞内で合成されたタンパク質由来のペプチド)を認識することで活性化されます。
この抗原認識を起点として、CD8⁺ T細胞はパーフォリンおよびグランザイムの放出、あるいは Fas リガンドを介した経路によって標的細胞を直接破壊します。
その結果、病原体が細胞内で複製・生存するための環境そのものが除去され、ウイルス感染の拡大や持続が抑制されます。
この MHC class I 依存的な抗原提示機構は、細胞内で増殖する病原体に対する防御において不可欠な仕組みです。
サイトカインネットワーク
細胞性免疫は、単一のサイトカインによって成立するものではなく、複数のサイトカインが相互に連携するネットワークとして機能しています。
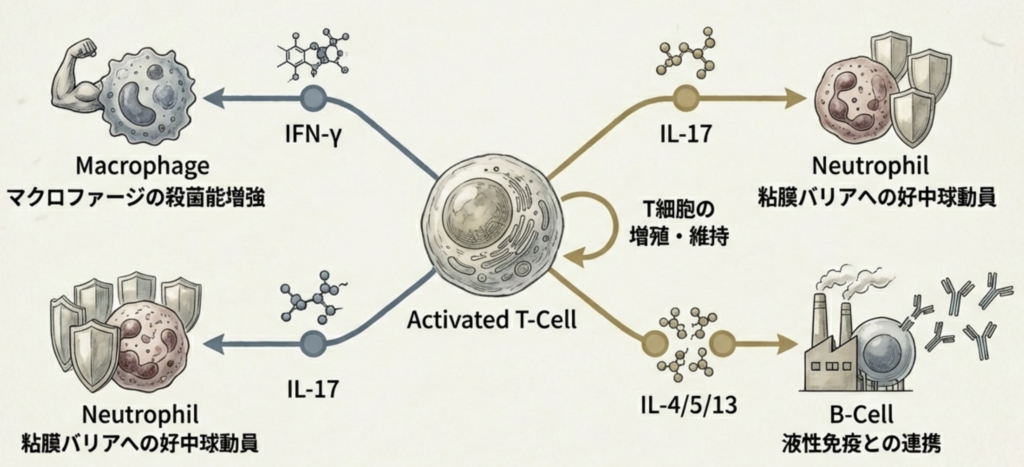
IFN-γ はマクロファージ活性化と抗菌能増強を担い、IL-2 はT細胞自身の増殖・維持に不可欠です。IL-17 は粘膜バリアにおける炎症応答を介して好中球動員を促進します。
さらに、IL-4、IL-5、IL-13 は Th2 細胞を介して B細胞活性化や抗体産生を促進し、IL-21 は濾胞性ヘルパーT細胞(Tfh)を介して胚中心形成と免疫記憶形成に関与します。
加えて、TNF-α は炎症反応の増幅や感染局所での免疫細胞活性化に寄与します。
これらのサイトカイン同士が協調することで、細胞性免疫を中心としつつ、液性免疫や自然免疫とも連動した感染制御が成立しています。
3. 細胞性免疫不全が形成される臨床状況(Host / Environment)
細胞性免疫不全は、原疾患そのものに加え、高度に発展した抗がん剤治療や免疫抑制剤によって人為的に形成される場面が増えてきています。
メンデル遺伝型マイコバクテリア易感染症、ジョブ症候群、IPEX症候群、ディジョージ症候群などの先天性免疫不全症も存在しますが、ここでは主に後天的に形成される細胞性免疫不全について解説します。
原疾患・治療に起因する細胞性免疫障害
1. 造血幹細胞移植(HSCT)
移植前処置や移植片対宿主病(GVHD)予防・治療(移植後シクロホスファミド、ステロイド、シクロスポリン、タクロリムス、MMF、ルキソリチニブ、イブルチニブなど)によって胸腺機能が障害され、細胞性免疫回復に時間がかかります。この期間、患者はCMV再活性化、EBV再活性化(移植後リンパ増殖性疾患)、アデノウイルス・BKウイルイスなどの生命を脅かすウイルスの再活性化や、血球生着後の市中獲得型感染症の脅威に晒されます。
2. T細胞枯渇・疲労
移植前処置や白血病の救援化学療法に用いられるプリンアナログであるフルダラビン、インドレントリンパ腫で主に使用されるプリンアナログとアルキル化薬のbifunctionalな機能を有するベンダムスチン、GVHD予防目的で使用されるシクロホスファミドや抗胸腺グロブリン、さらに CD52抗体であるアレムツズマブなどはT細胞を強力に枯渇させ、後天性免疫不全症候群(AIDS)に類似した深い免疫不全状態を形成します。また、CAR-T細胞療法では投与前にリンパ球除去療法を行うことが一般的ですし、二重特異性抗体では長期使用する薬剤も多く、T細胞疲弊を起こし長期的な細胞性免疫不全を招きます。
3. 高用量・長期ステロイド
高用量または長期のステロイド投与は、好中球の接着能を抑制することで末梢血中好中球数を相対的に増加させますが、炎症局所への集積を阻害し、T細胞活性化やマクロファージの殺菌機能を強力に抑制します。
教科書的な記載として、ニューモシスチス肺炎の予防はプレドニンを20 mg/日以上、2週間以上投与する場合に開始する、という基準が存在します。
しかし、がん治療においては抗がん剤レジメンや制吐剤として間欠的にステロイドが投与される場合も多く、この場合にもニューモシスチス肺炎を発症するリスクがあるため注意が必要です。
ステロイドは長期使用による毒性があり代替薬へ切り替えていくことが一般的(corticosteroid sparing)ですが、多くの場合その代替薬も細胞性免疫を抑制するため、細胞性免疫障害は持続します。
4. 分子標的治療薬
- JAK-STAT 阻害薬(ルキソリチニブなど):
JAK-STAT経路は、サイトカインシグナル伝達の中心的役割を担っています。
ルキソリチニブはこの経路を阻害することで、炎症性サイトカインを強力にダウンレギュレーションし、樹状細胞、NK細胞、およびCD4⁺ T細胞の機能を広範に抑制します。
この強力な細胞性免疫の抑制により、宿主は封じ込めていた病原体を制御できなくなり、結核・B型肝炎ウイルス(HBV)の再活性化のリスクが著明に高まります。
- BTK 阻害薬(イブルチニブなど):
イブルチニブは当初、B細胞受容体シグナルを標的とするB細胞特異的な薬剤(液性免疫への影響)と考えられていました。
しかし臨床的には、好中球数などの「数」が保たれていても、単球や好中球のBTK経路を介した殺菌能や遊走能を直接阻害することが判明しています。
このような「質的な好中球機能不全(functional neutropenia)」を引き起こす結果、細胞性免疫の不全とも相まって、侵襲性アスペルギルス症やニューモシスチス肺炎(PJP)といった、通常は自然免疫や細胞性免疫で制御されるはずの日和見感染症リスクが急上昇します。
特にステロイドとの併用や、前治療歴(慢性リンパ急性白血病に対するフルダラビンでの治療後など)によってこれらのリスクがさらに増幅されるため注意が必要です。
二次性・機能的T細胞不全
1. HIV感染
HIV感染は、CD4⁺ T細胞を選択的に減少させ、日和見感染症のリスクを著明に増大させます。また、持続的な抗原曝露により、CD8⁺ T細胞がエフェクター機能を失う「疲弊(exhaustion)」が進行し、PD-1やCTLA-4といった免疫逃避性分子の発現が亢進することで、感染制御がさらに困難となります。
2. 低栄養・高齢
宿主の栄養状態は免疫と深く関わりがあり、低栄養(特に鉄欠乏)はT細胞機能を直接障害するだけでなく、好中球の殺菌能も著しく低下させます。
加齢に伴う胸腺退縮(thymic involution)は、新規ナイーブTリンパ球の供給能力を低下させ、T細胞レパトア(多様性)の維持を妨げることで、加齢に伴う局所免疫の低下や感染リスクの増大を招く生理的要因となります。
3. 免疫調節異常
特定のサイトカインに対する自己抗体の存在は、後天的な免疫不全状態を形成します。
なかでも抗GM-CSF抗体は、好中球やマクロファージの殺菌能・走化性に不可欠なGM-CSFを中和し、単球におけるSTAT5シグナル伝達を阻害します。
この機序により、肺胞マクロファージの機能が障害され、自己免疫性肺胞蛋白症(aPAP)を発症するほか、本来は免疫正常と考えられていた患者においても、クリプトコッカス症(特に Cryptococcus gattii)やノカルジア症などの重篤な日和見感染症を発症します。
4. 細胞性免疫不全と関連す病原微生物
病原体が主としてどの免疫学的区画(細胞質、貪食胞内、あるいは細胞外)を生存・増殖の場として利用するかを理解することは、それを制御するために必要な免疫経路(CD4⁺ T細胞/CD8⁺ T細胞/好中球など)を予測する上で極めて重要です。
- エンドソーム/液胞内病原体 (Endosomal / Vacuolar Pathogens)
マクロファージなどの食細胞に貪食された後、ファゴソームやファゴリソソームと呼ばれる細胞内の区画に存在し、そこを主な生存の場とする病原体群です。
これらの制御には、IL-12/IFN-γ 軸に依存した CD4⁺ T細胞(Th1)とマクロファージの協調的活性化が不可欠です。
マイコバクテリア(結核菌・非結核性抗酸菌:NTM)
ファゴソーム内で生存・増殖し、肉芽腫形成を介した「疾患の封じ込め(disease containment)」の対象となります。
この経路のシグナル抑制下では、低病原性抗酸菌であっても播種性感染を来します。
サルモネラ(特に非チフス性サルモネラ)
食細胞内の液胞に局在し、IFN-γ によるマクロファージ活性化が低下すると、細胞内増殖を許し、菌血症や播種性感染へと進展します。
トキソプラズマ(Toxoplasma gondii)
Th1 細胞由来 IFN-γ が制御の要であり、細胞性免疫不全下では脳膿瘍や播種性疾患として再活性化します。
地域流行型真菌(ヒストプラズマ、コクシジオイデス)
マクロファージ内での生存と肉芽腫形成を通じて制御されていますが、細胞性免疫不全下ではこの封じ込めが破綻し、致死的な播種性感染へと進展します。
※ クリプトコッカス(Cryptococcus spp.)
マクロファージ内で一時的に生存可能であり、肉芽腫様制御を受けますが、主要な増殖ニッチは細胞外です。
そのため、生物学的には「典型的細胞内寄生真菌」ではなく、Th1 依存的免疫監視・制御に強く依存する病原体として理解するのが適切です。
- 細胞質内病原体 (Cytoplasmic Pathogens)
貪食胞から脱出し、宿主細胞の細胞質で直接複製する病原体群です。
細胞質内では殺菌機構が限られるため、防御は主に MHC class I を介した CD8⁺ T細胞による感染細胞の排除(細胞傷害)に依存します。
リステリア(Listeria monocytogenes)
細胞質内で増殖し、抗体や補体といった液性免疫から逃避します。
そのため CD8⁺ T細胞による排除が重要であり、T細胞機能が低下した患者では敗血症や髄膜炎を来します。
ウイルス(細胞内複製・免疫監視型)
宿主細胞内でタンパク質合成を行うため、CD8⁺ T細胞の主要な標的となります。
特にヘルペスウイルス群(CMV、EBV、VZV)は感染後に臨床的潜伏(clinical latency)を確立し、T細胞による持続的免疫監視(surveillance)によって抑制されています。
この監視が低下すると、CMV肺炎・網膜炎や、EBV による移植後リンパ増殖性疾患(PTLD)などが顕在化します。
EBV は IL-10 ホモログをコードするなど、多層的な免疫回避機構を有します。
- 主として細胞外で増殖する病原体 (Extracellular Pathogens with Immune Dependency)
主な増殖部位は細胞外ですが、特定の免疫回路への強い依存性を持つ病原体群です。
糸状菌感染症(アスペルギルス、ムーコル)
好中球による直接的排除が防御の中核であり、その有効な動員・活性化には Th17 細胞(IL-17/IL-22) や NK 細胞を含む統合的制御が必要です。
高用量ステロイドや BTK阻害薬(イブルチニブ) は、好中球の機能を質的に障害し、侵襲性真菌症のリスクを著明に高めます。
ムーコルでは鉄過剰状態やデフェロキサミン使用が増殖を助長し、致死的経過を取り得ます。
ニューモシスチス(Pneumocystis jirovecii)
CD4⁺ T細胞数低下が最大のリスク因子であり、HIV/AIDS に限らず、フルダラビン、JAK阻害薬、PI3K阻害薬使用下で顕在化します。
ノカルジア(Nocardia spp.)
環境由来菌であり、マクロファージ内生存能を有するものの、細胞内寄生を生活戦略とする病原体ではありません。
細胞性免疫低下、長期ステロイド使用、JAK阻害薬使用下などで新規感染として発症し、肺を起点に播種性感染を来します。
5. まとめ:細胞性免疫不全は「質的防御」の破綻である
細胞性免疫不全は、しばしば液性免疫不全と重なり合います。
B細胞活性化や抗体産生は CD4⁺ T細胞の制御を受けているため、T細胞障害は抗体応答低下に直結します。
また、CAR-T 療法などの新規治療はT細胞を標的としつつ、結果としてB細胞を広範に枯渇させ、重度の低ガンマグロブリン血症を引き起こします。


