1. バリアの破綻とは
血液悪性腫瘍含むがんの化学療法では骨髄抑制を起こすことが一般的です。
しかし、化学療法に伴う免疫不全 = 好中球数減少と単純に捉えることには限界があります。
多くの抗がん剤は好中球数を減少させるだけでなく、皮膚や粘膜といった生体バリアを含む複数の防御レイヤーを同時に障害します。
したがって、殺細胞性抗がん剤による免疫不全を好中球数減少という単一の要素に還元して理解することは、病態把握や臨床推論をかえって困難にします。
感染症成立を規定する「病原体(Agent)」「患者背景(Host)」「環境(Environment)」という三要素の枠組みにおいて、バリアは微生物の侵入を物理的に阻止する「第一線の防御壁(first line of defense)」として、極めて決定的な役割を担っていることはこれまでも述べてきました。
皮膚、消化管、呼吸器、尿路などの上皮構造は、感染症成立を最も早期の段階で左右する重要な要素です。
ただし、生体バリアは単なる物理的な「壁」ではありません。
皮膚や粘膜は、殺菌成分を含む分泌物、分泌型IgA、さらには常在細菌叢(microbiota)による栄養競合や定着阻止機構と密接に連携し、環境変化に適応する免疫器官として機能しています。
これらの物理的・生理的・免疫学的機構が協調することで、感染症成立に対する最重要の防衛ラインが形成されています。
本項では、がん治療が生体バリアに与える影響と、それに伴う感染症リスクの変化について解説します。
2. 生体バリアの構成:physical barrier と mucosal barrier
ヒトの皮膚(physical barrier)は、角質層による物理的遮断に加え、皮脂の酸性度、乾燥環境、汗に含まれる塩分、抗菌ペプチドなどを通じて微生物の定着や増殖を抑制します。
一方、粘膜(mucosal barrier)は、上皮構造に加えて粘液分泌、線毛運動、消化酵素などが協調して機能します。
さらに重要なのが、常在細菌叢(microbiota)の存在です。
物質の産生を通じて病原体の定着を阻止し、「定着抵抗性(colonization resistance)」を発揮します。
加えて、上皮細胞自体もパターン認識受容体(PRR)を介して微生物を感知し、サイトカインやケモカインを放出することで、後続の自然免疫・獲得免疫応答を動員します。
PRRをコードする遺伝子の多型による炎症制御が重度の腸管移植片対宿主病(GVHD)のリスク増加と関連する可能性が報告されていることは前述(#### 患者背景(Host)から考える感染症リスク)しましたが、生体バリアは多層的・統合的な防御システムとして機能しています。
3. 医療介入によるバリア破綻
抗がん剤、特に血液内科で扱う処置・強力な治療は、生体防御の第一線であるバリアを破綻さるリスクが非常に高いです。
皮膚バリアにおいては、針刺しや中心静脈カテーテル(CVC)の挿入が角質層を直接的に突破し、コアグラーゼ陰性ブドウ球菌などの皮膚常在菌が血流へ侵入する経路を形成します。
粘膜バリアについては、化学療法や放射線治療が細胞分裂の盛んな口腔・消化管上皮を障害し、粘膜バリア障害(mucosal barrier injury:MBI)を引き起こします。
MBIが生じると、細胞間を結ぶタイトジャンクションが破綻し、粘膜透過性が亢進します。
その結果、本来は管腔内に限局している微生物が血流へ移行するトランスロケーションが起こり、菌血症を起こすことがあります。
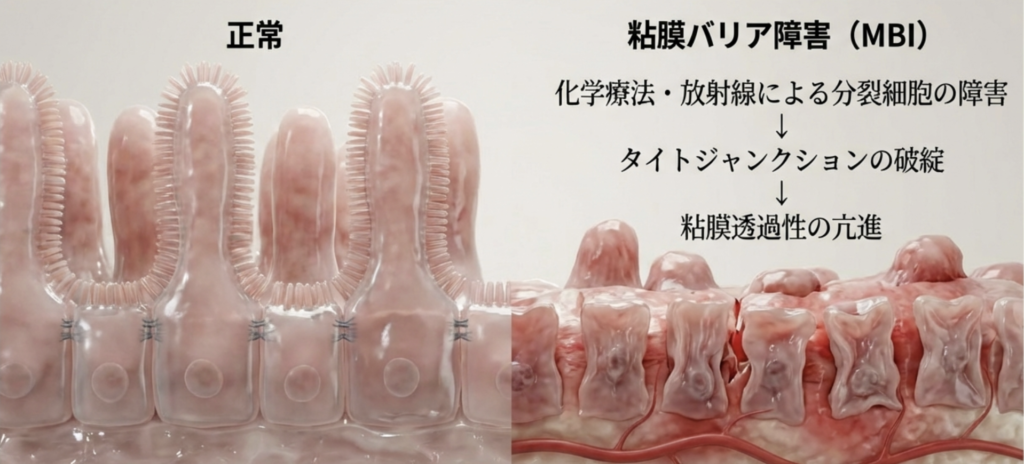
すなわち、治療介入そのものが感染症の「入口」を形成しているのです。
4. 粘膜バリア障害(MBI)の病態生理
血液悪性腫瘍患者におけるMBIは、生体防御の重大かつ早期の破綻点であり、その病態はStephen T. Sonisが提唱した5段階モデルで説明されます。
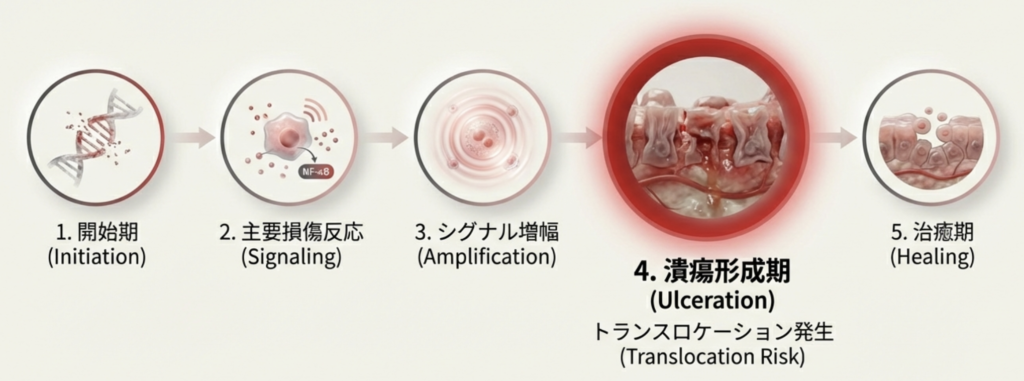
まず、化学療法や放射線により活性酸素が生成され、上皮細胞死が誘導される「開始期」が生じます。
続いてNF-κBが活性化され、TNF-α、IL-1β、IL-6などの炎症性サイトカインが産生される「主要損傷反応」が起こります。
この炎症反応は「シグナル増幅」を経て、臨床的な口内炎や腸炎を呈する「潰瘍形成期」に至ります。
この段階ではタイトジャンクションの損傷により粘膜透過性が高度に亢進し、微生物トランスロケーションが顕在化します。
造血幹細胞移植(HSCT)では、MBIの持続期間が好中球減少と同様に感染リスクを上昇させることが知られています。
最終的に、上皮が再形成される「治癒期」に至ります。
5. バリア破綻と関連する病原微生物
バリア破綻に伴う感染症は、解剖学的部位により特徴的な原因微生物の分布を示します。
皮膚では、CVC挿入部などを起点としてコアグラーゼ陰性ブドウ球菌、黄色ブドウ球菌、カンジダ属が重要です。
口腔粘膜では、MBIを介してViridans群連鎖球菌(VGS)、Rothia属、Capnocytophaga属などが菌血症の原因となります。
消化管では、大腸菌や緑膿菌(Hospital aquired)などのグラム陰性桿菌に加え、カンジダ属、Clostridium septicumなどが臨床的に問題となります。
これらの微生物は、宿主の防御機構が保たれている状況下では病原性を発揮しにくい一方で、宿主のバリア破綻によりその病原性が顕在化する宿主依存性の病原体です。
すなわち、感染症の成立は微生物固有の病原性のみで決まるものではなく、宿主側のバリア機能や免疫状態、さらには医療介入を含む環境因子との相互作用によって相対的に規定されます。
6. バリア破綻と好中球減少:役割の異なる二つの防御障害
ここまで述べてきたように、がん治療に伴う感染症リスクは、単一の防御機構の破綻によって説明できるものではありません。
特に臨床上重要なのは、バリア破綻と好中球減少が「同じ自然免疫の障害」ではあるものの、感染成立において果たす役割が本質的に異なるという点です。
バリアは、微生物の体内侵入そのものを阻止する「侵入防御」の役割を担います。
一方、好中球は、侵入を許した微生物を速やかに排除する防御機構の中心的存在です。
両者は連続した防御機構の一部であり、どちらか一方が破綻すれば感染症リスクは上昇しますが、どの段階で破綻が生じているかによって、感染症の様相や臨床推論の焦点は大きく異なります。
臨床的には、好中球数の回復に伴って感染リスクは一般に低下します。
しかし、MBIの持続期間が、特に造血幹細胞移植(HSCT)においては、好中球減少以上に感染リスクを強く高めることがあります。
末梢血上で好中球数が回復しても、上皮の再生やタイトジャンクションの再構築には、上皮幹細胞の回復速度に依存した一定の時間を要します。
その間は、微生物が血流へ侵入しやすい、トランスロケーションが生じやすい状態が持続します。
造血幹細胞移植では、前処置、免疫抑制療法、GVHDなどが重なり、バリア障害と好中球機能低下、さらには獲得免疫の障害が時間的にずれながら重層的に存在します。
このため、「好中球が何個あるか」だけではなく、『今現在、どの免疫がどのような組み合わせで、どの程度障害されているか、今後どのような変化をしていくか』を、経時的に捉える必要があります。
また、繰り返しにはなりますが、免疫不全感染症の臨床推論において”臓器”は、原因そのものではなく、病原体・宿主・環境という三要素の相互作用によって障害が顕在化する「フィールド」として位置づけられます。
このフィールドが現在どの段階にあるのかを意識的に捉えることも、適切な診断とマネジメントにつながります。
7. まとめ
生体防御を「バリア・好中球・細胞性免疫・液性免疫」の4層構造で捉えた場合、バリアは侵入を阻止する最初の障壁かつ不可欠な防御レイヤーです。
この層のがん治療による破綻は最も遭遇する事象の一つであり、常に念頭に入れておかなければならない免疫不全です。


