1. 液性免疫とは何が欠損するのか
液性免疫は、B細胞、抗体(免疫グロブリン:Ig)、および補体システム、とりわけ古典経路によって構成されています。
これらのいずれかが欠損、あるいは機能不全に陥ると、宿主は特定の病原体に対する防御能力を著しく失います。
細胞性免疫と異なり、液性免疫が主に担うのは細胞外で増殖する細菌、特に莢膜を有する細菌や、毒素、さらに細胞へ侵入する前段階の一部のウイルスに対する防御です。
液性免疫不全では、抗体による中和が成立せず、ウイルスや毒素が標的分子に結合するのを阻止できなくなります。
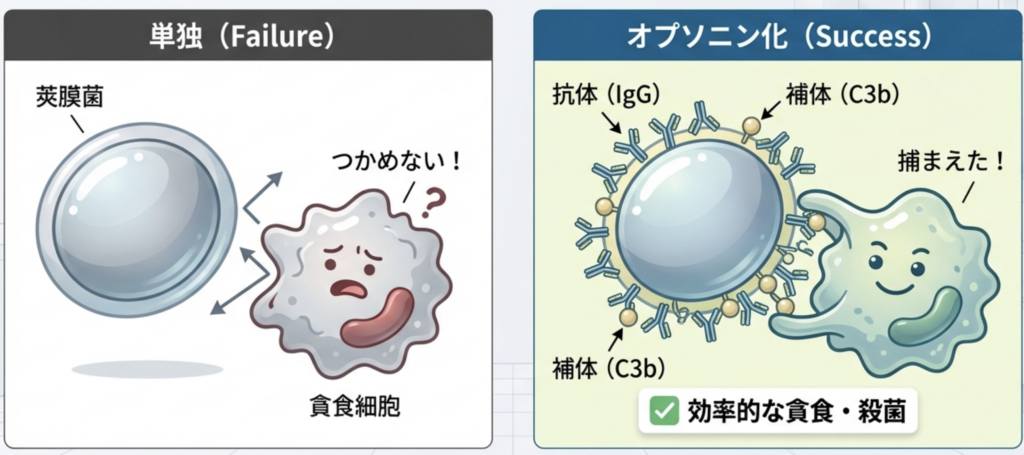
また、病原体表面への抗体や補体(C3b)の付着が不十分となることで、食細胞による取り込みが促進されない、いわゆるオプソニン化不全が生じます。
さらに、抗原抗体複合体を起点とする補体古典経路が活性化されないため、膜攻撃複合体(MAC)による直接的殺菌や、炎症細胞の効率的な動員も障害されます。
同じ獲得免疫であり病原体特異性を持つものの、この点で液性免疫不全は細胞性免疫不全と明確に区別されます。
T細胞機能の低下がウイルス、真菌、マイコバクテリアといった細胞内寄生体への易感染性をもたらすのに対し、液性免疫不全では、細胞外で増殖する微生物による反復性感染が臨床像の中心となります。
2. 抗体のエフェクター機能と感染防御
抗体は単に病原体を認識するだけでなく、他の免疫機構と連携することで感染防御を成立させます。
抗体が病原体表面に結合することで、宿主細胞への侵入や毒素の作用を物理的に阻止する中和が生じます。
また、IgGのFc領域は食細胞上のFcγ受容体と結合し、病原体の貪食を促進します。
これに加えて、抗原に結合したIgMやIgGは補体第1成分であるC1qを引き寄せ、補体古典経路を活性化します。
さらに、抗体で標識された標的細胞は、NK細胞などによって抗体依存性細胞傷害(ADCC)を受けます。
抗体クラスごとに役割も異なります。
IgGは血清中に最も多く存在し、血管外組織へも移行することで全身防御を担い、胎盤を通過して胎児に免疫を付与する唯一のクラスです。
IgMは感染初期に産生される五量体で、極めて強力な補体活性化能を持ちます。
IgAは主として粘膜表面に分泌され、病原体の付着や侵入を阻止する役割を果たします。
莢膜菌が有する多糖体抗原はタンパク質ではないためペプチドを生成できず、T細胞を刺激することができません。そのため、B細胞はT細胞からの重要な「第2の信号(CD40Lやサイトカインによる助け)」を受け取ることができません。 B細胞がIgMからより効果的なIgG(特に多糖体防御に重要なIgG2サブクラス)へのクラススイッチを行うには、T細胞との相互作用が不可欠です。長期的な免疫を担う記憶B細胞の形成もT細胞に依存しているため、多糖体単体では持続的な免疫が得られにくくなります。
そのため、小児、脾臓摘出後や特定の免疫不全状態では、莢膜菌に対する防御が不十分となります。
3. 液性免疫不全の病態分類
3.1 原発性(先天性)
原発性液性免疫不全は遺伝的欠損により生じ、多くの場合、母体由来抗体が消失する乳幼児期以降に発症します。
X連鎖無γグロブリン血症では、BTK遺伝子異常によりB細胞分化が停止し、すべての抗体クラスが著減します。
共通可変性免疫不全症(Common Variable Immunodeficiency:CVID)ではB細胞数が保たれることもありますが、抗体産生能が低下し、思春期以降に発症する例が多く見られます。
選択的IgA欠損症は最も頻度の高い免疫不全で、多くは無症状ですが、呼吸器感染や自己免疫疾患を合併することがあります。
高IgM症候群では、CD40/CD40L軸の異常によりクラススイッチが障害され、IgM以外の抗体が産生されません。
3.2 二次性(後天性)
二次性液性免疫不全は、基礎疾患や治療の結果として生じます。
多発性骨髄腫(MM)、慢性リンパ性白血病(CLL)、およびワルデンストレームマクログロブリン血症などでは、正常な抗体産生が抑制され、液性免疫の障害が引き起こされます。
また、リツキシマブなどの抗CD20抗体によるB細胞除去、二重特異性抗体・CAR-T細胞療法による低ガンマグロブリン血症、造血幹細胞移植後の免疫回復遅延も重要な原因です。
4. 液性免疫不全と関連す病原微生物
液性免疫不全においては、莢膜を有する細菌(肺炎球菌、インフルエンザ菌、髄膜炎菌)の排除が困難になります。
これらの細菌の駆逐には、IgG2サブクラス抗体や補体(C3bなど)が標的に結合する「オプソニン化」が不可欠だからです。
抗体や補体(特にC1、C2、C4などの古典経路成分)が欠損すると、食細胞が細菌を効率的に捕捉・殺菌できなくなります。
その結果、副鼻腔炎や中耳炎、肺炎といった再発性の呼吸器感染症に加え、髄膜炎などの侵襲性感染症を繰り返すことになります。
また、選択的IgA欠損症などにより粘膜免疫が損なわれると、腸管における防御機能が著しく低下します。本来、分泌型IgAは病原体の運動性を抑制し、上皮細胞への接着や毒素の結合を物理的に阻止する役割を担っています。 この防御壁が失われることで、ジアルジア(Giardia)などの原虫や、サルモネラ、シゲラ、カンピロバクターといった腸管病原体の定着・侵入を許しやすくなり、慢性的な下痢や吸収不良を引き起こします。
一部の症例では分泌型IgMによる代償的な輸送が行われるものの、それだけでは十分な防御に至らない場合も少なくありません。
さらに、ウイルス感染防御において抗体は、ウイルスが細胞内に侵入する前に結合して無力化する「中和」の役割を果たします。特に無ガンマグロブリン血症の患者において最も特徴的かつ深刻なのが、エンテロウイルスへの脆弱性です。X連鎖無γグロブリン血症(BTK欠損)では、エンテロウイルスが排除されずに中枢神経系へ感染が及び、慢性髄膜脳炎を引き起こして致命的な経過をたどることがあります。
B細胞障害性を持つリツキシマブで治療を受けた患者においてコクサッキーウイルスによる致命的な髄膜脳炎の発症が報告されており、B型肝炎が再活性化するリスクも指摘されています。また、稀ではありますがリツキシマブ投与後のJCウイルスによる進行性多巣性白質脳症(PML)発症例も報告されています。
発作性夜間ヘモグロビン尿症(PNH)は、造血幹細胞の遺伝子変異により、補体制御タンパク質であるCD55(DAF)やCD59(MAC抑制因子)が細胞表面に欠損することで生じ、C5に対するヒト化モノクローナル抗体であるエクリズマブが治療薬として挙がります。
しかし、この薬剤は薬理的に終末補体欠損状態を作り出すため、投与患者は先天性欠損症と同様に髄膜炎菌感染症のリスクが約2000倍に上昇します。そのため、エクリズマブの投与を開始する少なくとも数週間前には、四価髄膜炎菌結合型ワクチンの接種を完了させることが必須の管理手順となっています。
6. マネジメント
低ガンマグロブリン血症を伴う液性免疫不全の感染症予防において、主軸となるのは免疫グロブリン補充療法(IVIGまたはSCIG)です。血液領域では400mg/dLを閾値として免疫グロブリン補充療法が推奨されます。
莢膜被包菌はVPD(vaccine preventable disease)の一部を含んでおり、ワクチン接種が感染予防に有用です。前述のように、肺炎球菌などの多糖体抗原は、T細胞での認識が困難であるため、その防御には抗体や免疫記憶の形成が不十分なT細胞非依存性免疫に依存します。
しかし、多糖体にタンパク質(破傷風トキソイドなど)を結合させた結合型ワクチンを用いることで、B細胞が抗原を摂取・処理し、タンパク由来のペプチドをMHCクラスII分子を介してT細胞に提示することが可能になります。これにより、CD40/CD40L相互作用やサイトカインを介したT細胞の助けが引き出され、IgGへのクラススイッチと強固な免疫記憶が誘導されます。免疫不全者におけるワクチン接種戦略としてPCV13もしくはPCV15にPPSV23を併用することで免疫原性を高める戦略が取られていましたが、PCV20, 21の登場により、これらのワクチンを単独で使用することが可能となっています。
7. まとめ
液性免疫不全では、B細胞・免疫グロブリン・補体(特に古典経路)のいずれかが欠損・機能不全となり、ADCCとオプソニン化をベースとする防御が破綻します。
その結果、莢膜被包菌を含む細胞外細菌による反復性感染(副鼻腔炎、中耳炎、肺炎、敗血症、髄膜炎)を起こします。感染症の予防として、適切なタイミングでの免疫グロブリン補充療法や、ワクチン接種が重要です。



