免疫不全感染症においては、一般感染症よりも患者背景の因子を深く理解することが重要であることを前項で述べました。
宿主の免疫機構は、単一の要素によって成り立つものではなく、複数の防御機構が階層的に配置され、相互に連携しながら機能する統合的なシステムです。
各構成要素はそれぞれ独立した役割を担っていますが、いずれか一つが破綻すると、他の防御機構の機能にも連鎖的な影響が及び、特定の感染症リスクが顕在化します。
臨床感染症診療において理解しやすく、かつ実践的な枠組みとして、宿主防御機構は自然免疫である①バリア、②好中球と、獲得免疫である③細胞性免疫、④液性免疫の4つに分類します。
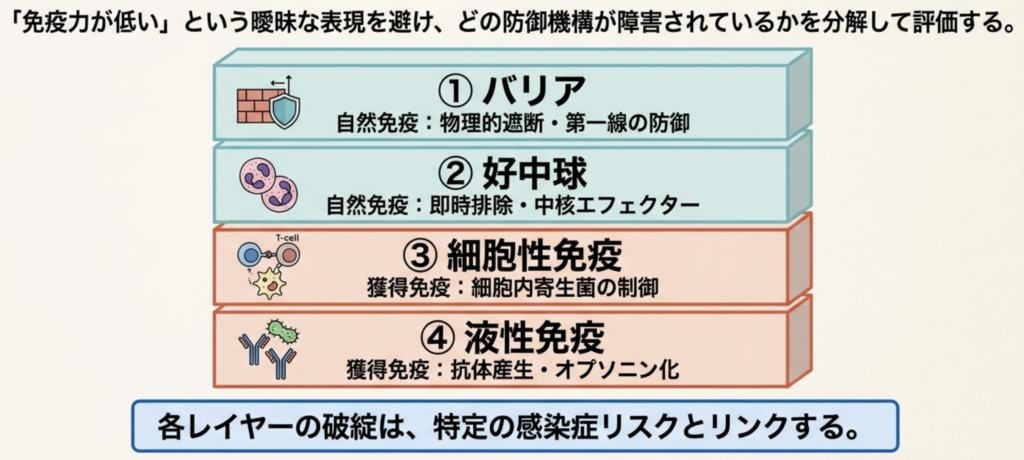
以下、それぞれの防御機構について、その免疫学的役割と臨床的意義を簡単に整理します。
① バリア:病原体侵入を防ぐ第一線の防御
バリアは自然免疫の最前線に位置する防御機構であり、皮膚や粘膜からなる「第一線の防御壁(first line of defense)」です。
皮膚、消化管、呼吸器、尿路の上皮構造は、病原微生物の体内侵入を物理的に遮断しています。
さらに、線毛運動、咳嗽反射、嚥下、排尿・排便といった生理的機構も、微生物を体外へ排除する重要な役割を果たしています。
加えて、正常細菌叢(microbiota)は、病原体との栄養競合や局所環境の制御を通じて、病原微生物の定着を抑制します。
抗がん剤治療や放射線治療、造血幹細胞移植前処置などによって生じる皮膚バリア障害、粘膜バリア障害(mucosal barrier injury; MBI)は、この防御機構を破綻させます。
その結果、本来は皮膚、腸管内、口腔内に局在する微生物が血流へ移行し、化学療法中に最も遭遇する感染症成立原因の一つです。
② 好中球:侵入した微生物を即座に排除する主力因子
好中球は自然免疫における中心的な細胞であり、走化、貪食、殺菌といった機構を通じて、侵入した微生物を迅速に排除します。
微生物の種類を選ばずに作用する点が特徴であり、感染成立初期の制御に不可欠です。
好中球減少や機能低下は、重症感染症および感染関連死亡に最も直結するリスク因子となり、発熱を来した場合は迅速な対応が必要です。
特に細菌感染症や侵襲性真菌症のリスクが上昇し、好中球数・機能の異常は急速な病勢悪化の主因となります。
③ 細胞性免疫:細胞内寄生病原体を制御
細胞性免疫は獲得免疫の一部であり、主にT細胞(CD4陽性・CD8陽性)によって生体防御全体を統合的に制御されます。
この防御機構は、ウイルス、抗酸菌、リステリア、ノカルジア、特定の真菌などの制御に不可欠です。
抗原提示細胞によって提示された抗原情報をもとにT細胞が活性化され、サイトカイン産生や細胞障害活性を介して感染制御が行われます。
細胞性免疫が低下すると、再活性化感染、日和見感染症のリスクが高まります。
④ 液性免疫:抗体による病原体排除
液性免疫も獲得免疫の重要な構成要素であり、B細胞から分化した形質細胞が産生する抗体を中心に機能します。
抗体は、病原体の中和、オプソニン化、補体活性化を介して、主に細胞外細菌の排除に寄与します。
特に、肺炎球菌、インフルエンザ菌、髄膜炎菌などの莢膜被包菌に対する防御は、液性免疫に強く依存しています。
また、B細胞の活性化や抗体産生はCD4陽性T細胞の制御を受けており、細胞性免疫と液性免疫は相互に密接な関係にあります。
まとめ
これら4つの防御機構は、いずれか一つが単独で障害される場合もあれば、複数が同時に、あるいは段階的に障害される場合もあります。
それぞれの防御機構が担う役割が異なるため、どの防御機構が障害されているかによって、感受性が高まる病原体の種類や感染症の臨床像は大きく異なります。
臨床において重要なのは、「免疫不全」という言葉を安易に用いて一括りに評価するのではなく、どの防御機構が、いつ、どの程度障害されているのかを具体的に把握することです。
防御機構の障害には”程度”はあり、軽度から重度まで連続的なスペクトラムとして存在していることを認識する必要があります。
自然免疫(バリア・好中球)と獲得免疫(細胞性免疫・液性免疫)は階層的に機能しますが、免疫不全患者では、これらの防御機構が同時に障害される、あるいは時間経過とともに連鎖的に破綻する状況が少なくありません。
そのため、基礎疾患や治療介入がどの防御レイヤーに、どの程度の影響を及ぼしているのかを総合的に評価することが、感染症リスクの予測、診断、そして管理の基本となります。


